№5, 2000 г.
© О.А.ГомазковЭндотелий — “эндокринное дерево” О.А.Гомазков
Олег Александрович Гомазков, доктор биологических наук, профессор,
главный научный сотрудник Института биомедицинской химии РАМН.Историческая преамбула
Вот интересно, откуда Шекспир знал это?
И влил в притвор моих ушей настой,
Чье действие в таком раздоре с кровью,
Что мигом обегает, словно ртуть,
Все внутренние переходы тела,
Створаживая кровь, как молоко,
С которым каплю уксуса смешали.“Гамлет”. Акт первый. Сцена пятаяБорис Пастернак в переводе почти не уклонялся от шекспировского текста. В тайне убийства Гамлета-отца на удивление похоже отражены знания физиологии той эпохи. Еще нет великой книги Уильяма Гарвея “Анатомическое исследование о движении сердца и крови”, где описано, как “кровь кружит в теле”. Еще нет знаний о процессах ее свертывания, но хорошо известны свойства растительных ядов и, в частности белены, которой был отравлен король. Уже сожжен на костре инквизиции богослов и врач Мигуэль Сервет, открывший легочное кровообращение. “Жизненный дух берет свое начало в левом сердечном желудочке, при этом <...> путь крови вовсе не пролегает через перегородку сердца, как принято думать, а чрезвычайно искусным образом гонится другим путем из правого сердечного желудочка в легкие”, — писал он в книге “Восстановление христианства...”, стоившей ему жизни.
В 1592 г. швейцарец Гаспар Бахин опубликовал свой труд “Theatrum Anatomicum”, где представлены картинки “полипа из сердца” [1]. Говоря сегодняшним языком, то были тромбиновые “слепки” полостей сердца и коронарных сосудов умершего человека, возникающие из “застывшей” крови. Эти экзотические образования, похожие на пучок корней диковинного растения, точь-в-точь соответствовали внутреннему устройству сердца и питающих его венечных артерий. Их форма отражала структуру “внутреннего тела” кровеносной системы — эндотелия, слоя клеток, выстилающего внутреннюю поверхность кровеносных и лимфатических сосудов, а также полостей сердца.
Зримое чудо
“С каждым днем занимаясь вскрытиями со все большим усердием, я с особой тщательностью изучал строение и функцию легких... При прямом падающем свете на поверхности легких в распущенном состоянии заметна чудесная сеть, которая кажется тесно связанной с отдельными пузырьками... Я придерживаюсь мнения, что вся масса крови, беспрерывно текущая по венам и артериям и состоящая из маленьких частиц, составлена из двух весьма сходных между собой жидкостей — беловатой, которая обычно называется сывороткой, и красноватой...” — так Марчелло Мальпиги впервые в 1661 г. описал микроциркуляторную систему легких и красные кровяные тельца.
Мальпиги работал с комбинацией простейших линз (Левенгук еще не изобрел микроскоп); успех достигался интуицией и усердием. Книга, в которой он описал свое открытие, приобрела большую известность; она логически завершала учение Гарвея. Мальпиги избрали почетным членом Английского Королевского научного общества. Однако на родине самого итальянца, в Болонье, его успех встретили враждебно. Однажды к нему явились двое замаскированных коллег в масках, в сопровождении нанятых хулиганов, которые избили 60-летнего профессора и разгромили его дом. Так своеобразно решалась тогда проблема “внешнего отзыва” и “черного рецензента”.
Ныне увидеть “зримое чудо” совсем несложно. На предметном столике бифокального микроскопа с разрешением в 800—1000 раз распластаем орошаемый физиологическим раствором препарат легких или брыжеечной ткани, пронизанный кровеносными микрососудами; сфокусируем и увидим в принципе то, что впервые рассмотрел Мальпиги, однако усиленное современной техникой и знаниями о системе микроциркуляции.
Крупные сосуды — артерии и вены, — разветвляясь, переходят во все более мелкие, постепенно превращаясь в ажурную сеть артериол, венул, капилляров, насыщающих каждый орган. Здесь происходят жизненно важные процессы обмена газов и продуктов питания организма. Средний диаметр капилляра человека 6—10 мкм, его длина около 750 мкм. Суммарное поперечное сечение капиллярного русла в 700 раз превышает сечение аорты, через которую кровь выбрасывается из сердца. Общая площадь сети капилляров составляет 1000 м2. Но если учесть, что в обмене также участвуют пре- и посткапиллярные сосуды, эта величина вырастает вдвое2. Вот здесь и разыгрываются десятки, быть может, сотни биохимических процессов, связанных с межклеточным обменом — его организацией, регуляцией и реализацией.
Работу микрососудов можно сравнить с микроциркуляторным маятником, обеспечивающим периодические задержки и промывки кровотока. В состоянии покоя функционирует не более четверти всех капилляров; при тяжелой физической работе их число увеличивается в 1.5 раза; при воспалении, атеросклерозе, нарушениях гемодинамики — снижается до величин, функционально недостаточных.
Есть еще одна особенность. В процессе жизнедеятельности физиологические системы работают неравномерно. Поел человек, и значительная доля крови направляется к органам пищеварения; занят интенсивной мыслительной деятельностью — мозговые структуры нуждаются в наибольшем снабжении кислородом, питательными веществами, пластическими материалами; выполняет физическую работу — системная гемодинамика и микроциркуляция мышц, сердца, легких обретают статус наибольшего обеспечения. Господствует рациональный физиологический закон: получает в первую очередь тот, кто в этом сейчас более всего нуждается. Старый купеческий принцип: “Всем сестрам — по серьгам!” — для природы неприемлем. В организме действует строгая и целесообразная избирательность, определяемая потребностями работающих систем. И если мы ведем речь о микроциркуляции, в глубинах которой происходят фундаментальные обменные процессы, то организация такой избирательности (т.е. перераспределение зон кровообращения) должна регуляторно обеспечиваться на рубеже кровь—стенка сосуда, где и находится эндотелий — “внутреннее тело” гемодинамики.
“Maestro of the blood circulation”
Говоря о сосудистой системе, было бы примитивным упрощением иметь в виду только крупные и мелкие пронизывающие тело “трубочки”, которые служат механическим “кровепроводом”... Кровь, за 40—60 с обегающая все уголки живого тела, помимо эритроцитов, главных носителей кислорода и углекислоты, содержит многие другие компоненты. Тромбоциты, похожие на миниатюрные лепешечки, — клетки, начиненные биологическим материалом, который необходим для “ремонтных работ” в сосудистой стенке. Не соответствуя общей стремительности потока, лениво перекатываясь по внутренней стенке, движутся лейкоциты. Они выполняют охранную миссию, обладая особой чувствительностью ко всему чужеродному. Здесь же макрофаги, похожие на растрепанные цветочные бутоны, — клетки иммунной защиты. А также системы белков, ферментов, гормонов, низкомолекулярных продуктов — целый сонм биологически активных веществ, синтезируемых или выбрасываемых в кровь из тканей.
Для сохранения равновесия в системе гемодинамики и для поддержания транскапиллярного обмена есть несколько условий, в реализации которых участвуют как химические факторы сосудистой стенки, так и перечисленные клетки крови.
Во-первых, — определенный уровень гидростатического давления в сосуде, без чего невозможны непрерывное движение крови и обменная функция между кровью и тканями.
Во-вторых, — непрерывность кровотока. Спазм сосуда, образование микротромбов, скопление клеток в каком-то участке микроциркуляторного ложа должны устраняться незамедлительно.
В-третьих, — репарация поврежденной сосудистой стенки; включение биохимических и физических механизмов; активация тромбоцитов и фермента тромбина, образование “заплаток” из фибриновых волокон, спазм микрососудов.
Эти условия формулируются как единое правило поддержания равновесия между тонусом сосуда, его физической целостностью и свойствами текущей крови, что некогда было определено как “гемо-васкулярный гомеостаз” [3]. Если свойства крови меняются — увеличивается число микроагрегатов, растет ее вязкость и, следовательно, возникает опасность нарушения транскапиллярной функции — в дело вступают биохимические системы, регулирующие течение транспортируемой жидкости и адаптивные изменения мышечного тонуса сосудов. Так постулировалась нами в 70-х годах роль калликреин-кининовой системы крови.
Наконец (в-четвертых), — регуляция транскапиллярной проницаемости. Существовавшее долгое время представление о пассивной роли микрососудов в обменных процессах рухнуло под лавиной новых фактов. В словаре нынешних специалистов фигурируют такие понятия как “микровезикуляция”, “пиноцитоз”, “интерстициальный градиент”, “скаффелдинг” (создание строительного каркаса), “ремоделирование мембран” и др. Эндотелий — мономерный слой пограничных клеток между кровью и мышечным слоем сосуда — оказывается важнейшей тканевой структурой, причастной к регуляции и реализации всех перечисленных функций.
В 1945 г. австралийский патолог Г.Флори, работавший в Оксфорде вместе с А.Флеммингом и Э.Чейном, получил Нобелевскую премию за пенициллин. Однако остались малоизвестными его последующие работы по изучению эндотелия. Используя электронную микроскопию, Флори установил, как макромолекулы диффундируют сквозь стенки артерий и вен различных органов. Он впервые обнаружил мембранные микроструктуры эндотелия и межклеточные соединения, участвующие в транспортных процессах; выяснил его роль в образовании атеросклеротических изменений сосудов. Работы Флори послужили основой сегодняшних представлений об эндотелии — ткани, ответственной за сопряжение множества процессов в системе кровообращения. Эти исследования привели к пониманию молекулярных причин патогенеза многих сосудистых заболеваний: атеросклероза, гипертонии, сердечной и почечной недостаточности, отеков. Возникло особое понятие (по сути новая клиническая форма — эндотелиальные дисфункции), объединяющее огромный спектр нарушений сердечно-сосудистой системы в целом.
По современным представлениям, эндотелий — не просто барьер или фильтр. Это — активный эндокринный орган, самый большой в теле, диффузно рассеянный по всем тканям. Он синтезирует субстанции, важные для контроля свертывания крови, регуляции тонуса и артериального давления, фильтрационной функции почек, сократительной активности сердца, метаболического обеспечения мозга. Контролирует диффузию воды, ионов, продуктов метаболизма. Реагирует на механическое воздействие текущей жидкости, кровяное давление и ответное напряжение, создаваемое мышечным слоем сосуда. Чувствителен к химическим и анатомическим повреждениям, которые могут приводить к повышенной агрегации и адгезии (прилипанию) циркулирующих клеток, развитию тромбоза, оседанию липидных конгломератов. “Маэстро кровообращения” — так именовал его нобелевский лауреат британский фармаколог Дж.Вейн. (Старинный словарь определяет “маэстро” как почетный статус дирижера оркестра или виртуоза-музыканта.)
Попробуем определить четыре уровня, по которым развивается биологическое и медицинское знание.
— Как устроено? — Анатомия органа, клетки, молекулярной структуры. Гален и Везалий начинали с исследования человеческого тела, его отдельных частей, соединяемых понятием “система”. Шлейден, Шванн, Вирхов сфокусировали знание на клеточной организации тела. Биохимия ХХ в. открыла макромолекулы — белки, липиды, нуклеиновые кислоты, составляющие базис живых структур.
— Как работает? — Физиология и биохимия. Необходимость понять, как “оно” (так устроенное) функционирует во взаимодействии. Исходно биохимия, на которой зиждется вся молекулярная анатомия живого, именовалась физиологической химией. В итоге, физиология — это философия живого, представление “так устроенного” в объеме взаимосвязей и противоречий.
— Почему поломалось? — Патофизиология и патология. В каком звене, в какой структуре произошел сбой? Здесь действуют принципы как частного, так и общего (системного) порядка, поскольку известные законы физиолого-биохимического устройства организма с той же конкретностью и мощью участвуют в сотворении болезни, “зла”.
— Как исправить? — Терапия, основанная на знании ключевых звеньев, усилением функции которых или, наоборот, ослаблением можно скоррегировать нарушенное равновесие. Вернуть работу органа, системы, цепи биохимических процессов к исходному и функционально необходимому балансу.
Эндотелий — “эндокринное дерево” (как устроено?)
Эндотелий, по классическому определению гистологов, — однослойный пласт специализированных клеток, выстилающих изнутри все сердечно-сосудистое дерево. Для человека среднего веса — это ткань с общей площадью в шесть теннисных кортов (эдакий “Уимблдон” со всеми запасниками) и весом около 1.8 кг. Один триллион клеток со сложнейшей “биохимической кухней”, включающей системы синтеза белков и низкомолекулярных веществ, рецепторы, ионные каналы.
Эндотелиальное дерево совсем не однородно в своей архитектуре. Его гетерогенность, соответствующая гетерогенности сосудистого ложа, зависит от размера, структуры, биохимической организации, функции данного органа. Эндотелий коронарных сосудов, легочный эндотелий, церебральный и др., хотя и схожи анатомически, но существенно различаются в генной и биохимической специфичности, типах рецепторов, наборе белков-предшественников, ферментов, трансмиттеров. Соответственно патологические явления также избирательно развиваются в популяциях эндотелиальных и сосудистых клеток: они неодинаково чувствительны к атеросклерозу, ишемическим нарушениям, развитию отека и др. Эти особенности весьма существенны при формировании эндотелиальных дисфункций и других патологий.
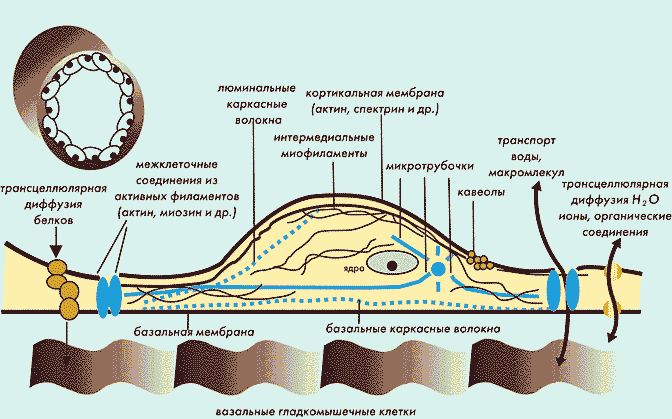
Поперечный срез сосуда (вверху слева) и микроструктура эндотелиальной клетки.
Интриги вокруг маленькой молекулы (как работает?)
Говоря о “биохимической кухне” эндотелия, можно перечислить не менее двух десятков (известных только на сегодняшний день) биологически активных веществ, синтезируемых и высвобождающихся в соответствии с функциональными потребностями. Функции эндотелия складываются как баланс регуляторных субстанций, определяющих целостную работу системы кровообращения (табл.1). Среди них факторы, контролирующие сокращение и расслабление мышц сосудистой стенки (т.е. ее тонус); участвующие в свертывании и фибринолизе (т.е. регуляции жидкого состояния крови и ее взаимодействии с сосудистой стенкой); контролирующие рост клеток (т.е. их восстановление и замещение); регулирующие воспаление (т.е. реакцию на уничтожение и изгнание чужеродного начала).
Таблица 1. Факторы, синтезируемые в эндотелии и регулирующие его функцию
Факторы сокращения и расслабления сосудистой стенки
КОНСТРИКТОРЫ ДИЛАТАТОРЫ Эндотелин
Ангиотензин-II
Тромбоксан (TXA2)
Простагландин Н2Оксид азота
Эндотелин
Простациклин (PGI2)
Эндотелиновый фактор деполяризации (EDHF)Факторы гемостаза и антитромбоза
ПРОТРОМБОГЕННЫЕ АНТИТРОМБОГЕННЫЕ Тромбоцитарный ростовой фактор (PDGF)
Ингибитор активатора плазминогена
Фактор Виллебранда (VIII фактор свертывания)
Ангиотензин-IV
Эндотелин-1Оксид азота
Тканевой активатор плазминогена (TPA)
Простациклин (PGI2)Факторы, влияющие на рост сосудов
СТИМУЛЯТОРЫ ИНГИБИТОРЫ Эндотелин-1
Ангиотензин-II
Супероксидные радикалыОксид азота
Простациклин (PGI2)
С-натриуретический пептидФакторы, влияющие на воспаление
СТИМУЛЯТОРЫ ИНГИБИТОРЫ Фактор некроза опухоли (TNF-alpha)
Супероксидные радикалыОксид азота Оксид азота (NO) среди физиологически значимых молекул — самая простая химическая структура, выполняющая однако роль конечной “инстанции” в ряду многих функций эндотелиальных клеток. Оксид азота присутствует во всех эндотелиальных клетках — независимо от размера и функции сосудов. В покое эндотелий постоянно секретирует определенные количества NO, поддерживая тонус артериальных сосудов. Большинство химических факторов, синтезируемых в эндотелии или циркулирующих с кровью, реализуют свое действие через NO.
Синтез NO усиливается при динамическом напряжении мышечных элементов сосуда, сниженном содержании кислорода в ткани, в ответ на выброс в кровь ацетилхолина, гистамина, норадреналина, брадикинина, АТФ и др. Образующиеся в эндотелии вещества находятся в функциональном равновесии с NO как часть системы обратной связи, поддерживающей статус сосудов в норме. Некоторые из них меняют свои физиологические эффекты на противоположные в сосудах с удаленным эндотелием или нарушенным синтезом NO. Такие эксперименты моделируют “механику” возникновения атеросклероза, развития коронароспазма или утолщения (гипертрофии) сосудистой стенки.
Оксид азота как эндотелиальный фактор расслабления был открыт в 1980 г. Р.Фешготтом и И.Завадски. При изучении релаксирующего эффекта ацетилхолина на артериальных гладких мышцах выявлялась некая эндотелиальная субстанция. Вещество синтезировалось из L-аргинина под действием фермента синтаза азота. Различают три ее изоформы, две из которых обнаружены в нервной ткани и в эндотелии; третья — во многих клетках иного типа (например, в почечных канальцах).
Оксид азота тормозит работу сократительного аппарата сосудистых гладкомышечных элементов; при этом активируется фермент гуанилатциклаза и образуется вторичный (скорее, “третичный”) посредник — циклический 3’-5’-гуанозинмонофосфат. NO препятствует адгезии циркулирующих тромбоцитов и лейкоцитов к эндотелию; эта функция сопряжена с простациклином, который препятствует агрегации и адгезии клеток. Синтез NO и соответственно его активность стимулирует брадикинин — полипептид, который образуется в крови под действием ферментов калликреина и XII фактора свертывания крови. Так, спустя почти 20 лет оказывается фактологически утвержденной наша идея о роли калликреин-кининовой системы в регуляции гемо-васкулярного гомеостаза — функционального равновесия реологического статуса крови и тонуса сосудов. Появились новые важные сведения о значении эндотелия и синтезируемых им регуляторных субстанций.
С помощью фармакологических средств выяснилась роль В2-кининовых рецепторов, находящихся на поверхности эндотелиальных клеток: их блокада тормозит вызываемое брадикинином расслабление сосудистых клеток (вазодилатацию) и высвобождение NO. Активность другого пептида — ангиотензина II, вызывающего сокращение (констрикцию) артериальных сосудов, угнетает оксид азота. И брадикинин, и ангиотензин II связаны с ангиотензин-превращающим ферментом (АПФ) [4]. Сегодня его роль в патологии сердечно-сосудистой системы оценивается весьма высоко: ингибиторы АПФ — одно из самых распространенных средств терапии таких заболеваний.
Сопряженность активности брадикинина с сопрягающими факторами. В2 — кининовый рецептор, PGI2 — простациклин, EDHF — эндотелиальный фактор гиперполяризации, цГМФ — циклический гуанозинмонофосфат, цАМФ — циклический аденозинмонофосфат.Эндотелин: новое имя со старым корнем
В 1988 г. японский исследователь М.Янагасава с коллегами опубликовали в “Nature” статью о новом эндотелиальном пептиде, активно сокращающем сосудистые клетки. Открытый фактор сразу стал предметом интенсивного изучения. Этот пептид, названный эндотелином, — сегодня один из самых популярных в списке биоактивных регуляторов. Только за последние два года ему посвящено 2.5 тыс. публикаций. Такой интерес связан с тем, что, во-первых, эндотелин — вещество с наиболее мощной сосудосуживающей активностью (изменения артериального давления вызываются дозами в 10–12—10–14 моля, т.е. одна миллионная часть миллиграмма!); а во-вторых, пептид образуется в самом большом эндокринном органе — эндотелии.
Эндотелин — крупная полипептидная молекула: 21 аминокислотный остаток, бициклическая структура, связанная сульфгидрильными мостиками. Его неактивный предшественник — “большой эндотелин”, содержащий 38 аминокислот, от которого специальный фермент “отрезает” собственно эндотелин5. В организме присутствуют несколько форм пептида, различающихся небольшими нюансами химического строения, но весьма несхожих по локализации в организме и физиологической активности.
Синтез эндотелина стимулируют тромбин, адреналин, ангиотензин, интерлейкин, клеточные ростовые факторы и др. Создается впечатление высокой сопряженности пептида с регуляторами различного происхождения. В большинстве случаев эндотелин секретируется из эндотелия “внутрь”, к мышечным клеткам, где расположены чувствительные к нему ЕТА-рецепторы. Меньшая часть синтезируемого пептида, взаимодействуя с рецепторами ЕТВ-типа, стимулирует синтез NO. Таким образом, один и тот же фактор регулирует две противоположные сосудистые реакции (сокращение и расслабление), реализуемые различными химическими механизмами.
Рецепторы эндотелина, как, впрочем, рецепторы любой биологически активной субстанции — особое устройство управления физиологическим актом, его ключевой механизм. Активный участок, включающий определенный набор аминокислотных остатков, специфически узнает своего “контрагента” (будь то пептид, гормон, медиатор) и после соединения с ним инициирует цепь трансмембранных реакций, необходимых для реализации физиологического эффекта. Для одного и того же вещества выявлены подтипы рецепторов, несхожие по клеточной локализации и запускающие “сигнальные” биохимические реакции. Налицо биологическая закономерность, когда одно и то же средство (тот же пептид, гормон, медиатор) регулирует различные физиологические процессы (табл.2).
Таблица 2. Подтипы рецепторов эндотелина-1: локализация, физиологические эффекты и участие вторичных посредников
РЕЦЕПТОР ТКАНЬ ЭФФЕКТ ПОСРЕДНИКИ ЕТА
ЕТВ2
ЕТА
ЕТВ1гладкая мышца сосуда
гладкая мышца сосуда
эндотелий
эндотелийконстрикция
митогенез (пролиферация)
высвобождение NO, PGI2, EDGF
высвобождение NO и других факторовфосфолипаза С
инозитолфосфат, диаглицерол
фосфолипазы C, D, A2
аденилат-гуанилатциклазыОгромный интерес к клиническому исследованию эндотелинов носит подчас эмоциональную тональность и нередко выражается в заголовках научных публикаций типа: “Эндотелин-1: курьез ученых или реальный виновник ишемической болезни сердца?”, “Антагонисты рецептора эндотелина: сердечные препараты будущего?”, “Артериальная стенка: новая фармакологическая и терапевтическая мишень”. Эндотелин рассматривается как маркер и “предсказатель” многих сосудистых патологий. Этот пептид оказывается причастным к: ишемической болезни сердца, острому инфаркту миокарда, нарушениям ритма сердца, атеросклеротическим повреждениям сосудов, специфическим сосудистым нарушениям (рестенозу вследствие коронарной ангиопластики), легочной и системной гипертензии, послеродовым сосудистым осложнениям, почечной патологии васкулярного гломерулонефрита, ишемическим повреждениям мозга (субарахноидальной геморрагии), неинфекционным легочным заболеваниям, диабету и др.
Двойной эффект эндотелия. ЕСЕ — эндотелин-превращающий фермент, ЕТВ и ЕТА — подтипы рецепторов, B-ЕТ — большой предшественник эндотелина, NO-S – синтаза оксида азота.Проблема эндотелиальных дисфункций (почему поломалось?)
Функции эндотелия складываются как баланс противоположно действующих начал: усиление—ослабление сосудистого тонуса, агрегация—дезагрегация клеток крови, увеличение—уменьшение числа сосудистых клеток. В каждом случае результат определяется концентрацией синтезируемых веществ, между которыми существуют строгая зависимость и равновесие.
Впрочем, равновесие своеобразное — асимметричное. Это не два плеча одного коромысла. Речь идет о сложном переплетении регулируемых физиологических эффектов. Здесь работает один из главных принципов биохимии и физиологии — организация противостояния, когда контроль действующего начала осуществляют, к примеру, ингибиторы ферментов, факторы фибринолиза, возбуждение тормозных нейронов и др.
В сосуде с “нормальным” эндотелием баланс всегда сдвинут в сторону поддержания вазодилатации — готовности противостоять усилению тонуса. Оно и понятно: активное начало определяется созданием напряжения в циркуляторной системе, созданием градиента, благодаря которому происходит обмен в тканях. Тому служит множество веществ, синтезируемых в крови, в эндотелии и в мышечных клетках. Поэтому механизм потребного усиления функции — повышения сосудистого тонуса и проницаемости — двойной: активация факторов “про” и ослабление факторов “контра”. Нередко это делается одним поворотом “двузубчатого ключа”: ангиотензин-превращающий фермент стимулирует образование ангиотензина II и разрушает его антипод — брадикинин. Пептид эндотелин, действуя через различные подтипы своего рецептора, приводит к сокращению или, наоборот, релаксации мышечных клеток.
Патологии, связанные с дисфункцией эндотелия, есть продолжение его “добродетелей”. Велик и разнообразен список заболеваний, имеющих эндотелий-зависимое происхождение, в значительной мере совпадающий с негативными эффектами пептида эндотелина. Исходная и развивающаяся “механика” этих болезней связана с нарушением дисбаланса эндотелиальных субстанций — нерегламентируемым усилением роли одних и ослаблением “оппозиционной” работы других. Здесь видится важный и совершенно новый подход: понимание болезни как развивающегося дисбаланса химических регуляторов, т.е. нарушения системы противостояния.
Заболевания, связанные с эндотелиновыми дисфункциями
атеросклероз, гипертоническая болезнь,
коронарная недостаточность,
инфаркт миокарда,
почечная недостаточность,
посттрансплантационная болезнь реперфузии,
диабет и инсулиновая резистентность, наследственные и приобретенные
нарушения обмена
(гиперхолестеролемия, гиперлипидемия и др.),эндокринные возрастные нарушения,
недыхательные легочные патологии (астма) и др.
Изучение функций эндотелия в нормальном организме и химических факторов его регуляции служат основой для постулирования такого взгляда. В целом, современное понимание патологии эндотелиальных дисфункций можно сформулировать как своеобразную “триаду зла”:
Васкулярная медицина-XXI (как исправить?)
- нарушение равновесия противоположно действующих начал;
- нарушение противостояния в системе регуляторных субстанций;
- возникновение “порочных кругов”, дисбалансирующих функцию клетки, органа, физиологической системы.
Это самый трудный на сегодня вопрос. Современная терапевтическая стратегия в отношении эндотелиальной патологии направлена на удержание или восстановление равновесия описанных выше факторов. В целом речь идет об ограничении действия одних эндотелиальных факторов, компенсации дефицита других и восстанавлении их функционального баланса. Например, нитрат-содержащие препараты компенсируют дефицит эндогенного NO; антагонисты Ca++ “сдерживают” активность ангиотензина II и эндотелина в гладких мышцах сосудов, облегчая вазодилататорный эффект NO; ингибиторы ангиотензин-превращающего фермента помимо снижения синтеза ангиотензина II препятствуют разрушению кининов; недавно появившиеся ингибиторы эндотелин-превращающего фермента и антагонисты рецепторов эндотелина-1 тормозят активность пептида. Однако базовое лечение эндотелиальных дисфункций пока отсутствует.
Появилось новое стратегическое понятие — васкулярная медицина. Ее основой служат базовые знания об эндотелии, могучем эндокринном органе, и процессах, проистекающих в его клетках, которые становятся теперь все более понятными, однако до сих пор не перестают удивлять своей сложностью.
Что делает ребенок с новой игрушкой? Он “изучает” ее, разбирая на палочки, колесики, винтики — интересно, как “оно устроено” — чтобы потом, когда станет взрослым, сделать лучшую.
Работа выполнена при поддержке РФФИ (грант 99-04-99322)
Литература
1 Die Chronik der Medizin / Red. H.Schott. Dortmund, 1993.
2 Алексеев О.В. Микроциркуляторный гомеостаз // Гомеостаз / Ред. П.Д.Горизонтов. М., 1981. С. 419—460.
3 Гомазков О.А. // Кардиология. 1973. №7. С. 130—144.