№10, 2003 г.
© Б.С. Баталин
Вред и польза шлаковых отвалов
Б.С. Баталин
Борис Семенович Баталин, доктор технических наук,
профессор кафедры строительных материалов и специальных технологий
Пермского государственного технического университета.Производство металлов из руд сопряжено с образованием значительного количество отходов. Такова уж технология - чтобы получить металл, используют топливо, плавни (флюсы), снижающие температуру плавления руды, вещества, извлекающие из нее и жидкого еще металла вредные для его качества примеси. Все эти ингредиенты в ходе выплавки образуют шлаки, весьма разнообразные по составу и свойствам.
О металлургических шлаках * многое известно, существует подробная классификация и обширная литература. Здесь же речь пойдет о свойствах, влиянии на окружающую среду, проблемах утилизации и области применения только одного типа шлаков - самораспадающихся (их иногда называют саморассыпающимися за способность превращаться в тонкий порошок при остывании).
* Один из их типов - сплав оксидов, обычно покрывающих поверхность жидкого металла при его выплавке.
“Месторождения” полезных ископаемыхЗа время существования металлургических заводов рядом с ними накопилось огромное количество шлаков (на одном только Чусовском их более 150млн т!). Давно известно, что даже старые, уже выведенные из эксплуатации отвалы, вредно влияют на атмосферу, гидросферу и почвенный покров окружающей местности, а через них - на состояние флоры, фауны и здоровье людей [1]. Поэтому ликвидация шлаковых отвалов сегодня стала одной из самых насущных задач охраны окружающей среды.
Утилизации шлаков посвящено множество разработок ученых, технологов, экологов. И в ряде случаев уже предпринимаются меры по переработке в строительные материалы: щебень, песок, вяжущие материалы. Задача эта весьма сложна, поскольку связана с технологическими, техническими и экономическими трудностями.
Во-первых, в одном и том же отвале часто складируются шлаки разных металлургических производств предприятия, например доменные, мартеновские и конвертерные. А состав и свойства шлаков в них неодинаковы. Меняются, кроме того, руды, флюсы, технология производства. Все это сказывается на составе и свойствах шлака.
Во-вторых, в отвале происходит механический распад шлака (крупные куски из-за медленных изменений фазового состава рассыпаются в порошок) и химический (силикатный, марганцовистый, железистый виды), вызванные внутренними и внешними причинами. Отдельные компоненты шлака могут взаимодействовать с дождевой и снеговой водой, образуя новые соединения, и тогда меняются его дисперсность и агрегатное состояние. За счет этого частицы могут фракционироваться по размеру, отвал становится слоистым. Состав и свойства шлака оказываются разными и по высоте, и по простиранию этой почти геологической структуры.
Естественно, что его переработка даже в щебень и песок затруднена: ведь одна часть отвала может быть вполне пригодна для получения таких строительных материалов, а другая - нет. Начатая уже утилизация может стать экономически нецелесообразной, предприятие понесет убытки.
Химический состав металлургических шлаков принято представлять в форме оксидов - SiO2, CaO, Al2O3, Fe2O3, MgO и т.д. Для характеристики свойств шлака наиболее важны два количественных соотношения: СаО / SiO2, (модуль основности) и SiO2 / Al2O3 (модуль активности). По величине первого модуля различают кислые (он меньше единицы), нейтральные (равен единице или близок к ней) и основные (>1) шлаки. Кроме оксидов в них всегда содержатся компоненты, многие из которых весьма ценны (соединения титана, ванадия, хрома, других нужных промышленности химических элементов), причем в количестве часто не меньшем, чем в природных рудах.
Фазовый состав шлака зависит в первую очередь от модуля основности. В кислых с наибольшей вероятностью образуется стекловидная фаза (особенно при резком охлаждении), в нейтральных и основных - кристаллическая. Ее чаще всего составляют силикаты и алюмосиликаты кальция и магния в форме минералов: псевдоволластонита, анортита, геленита, ларнита, монтичеллита, мервинита, ранкинита, мелилита. Нередки также шпинель, диопсид и др. Конечно, в шлаках с разным модулем основности преобладают вполне определенные минералы [2].
Модуль основности самораспадающихся шлаков близок к двум, поэтому стекловидная фаза в них не образуется даже при резком охлаждении. Из минералов же преобладает ларнит Ca2[SiO4] (в металлургической отрасли принята стехиометрическая запись состава минералов: ларнит обозначают 2CaO·SiO2 и называют ортосиликатом кальция). Такой шлак не способен твердеть при смешивании с водой, подобно тому как это происходит с портландцементом, одним из важнейших строительных материалов, хотя по химическому составу тот и другой весьма близки.
Почему твердеет цемент
Получение портландцемента начинается со спекания строго рассчитанной смеси из молотого известняка и глины в специальной печи при температуре 1450°С. О дальнейших стадиях нет необходимости рассказывать здесь, однако стоит упомянуть, что в производстве этого строительного материала предусмотрены добавки, например гипс, который регулирует схватывание будущего цемента, и активная минеральная добавка, повышающая его стойкость к некоторым видам коррозии.
Основу портландцемента, как и самораспадающегося шлака, составляют СаО, SiO2, Al2O3 и Fe2O3 (в качестве примесей могут содержаться MgO, K2O, Na2O и др.). Эти оксиды образуют четыре основных минерала с собирательным названием “клинкерные”. При контакте с водой они самопроизвольно вступают с ней во взаимодействие, в результате чего образуются кристаллические и коллоидные гидраты. Кристаллогидраты срастаются между собой в твердый, но хрупкий агрегат, а гелевидные придают ему пластические свойства, за счет чего существенно снижается хрупкость. Именно гидратные соединения способствуют превращению порошкового цемента в твердое тело. Его прочность на сжатие составляет 30, 40, 50 МПа, что соответствует маркам цемента “300”, “400”, “500”
Один из клинкерных минералов - ортосиликат кальция - может существовать в a-, b- и g-формах, т. е. полиморфных разновидностях. Первая из них образуется при температуре 1425° и в процессе медленного охлаждения переходит (через две промежуточные стадии) во вторую, а потом - в третью (рис.1). Если на второй промежуточной стадии минерал быстро охладить, он останется в виде b-формы, способной к гидратации и твердению. Переход b-формы в g-ортосиликат сопровождается сильным увеличением объема кристаллической решетки, поэтому минерал стремительно разрушается. Кристаллики быстро, в течение доли секунды, рассыпаются в тонкий порошок. Очень важно, что эти превращения обратимы, но за исключением одного: g-разновидность не переходит в b-форму ни при каких условиях, а может превратиться только в a-модификацию.
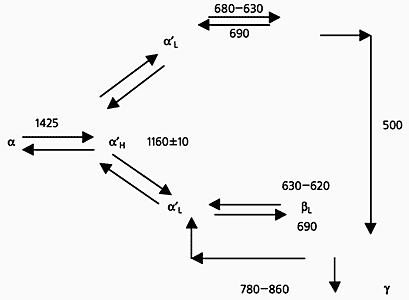
Рис. 1. Полиморфные превращения ортосиликата кальция.
a и a’ - промежуточные фазы; буквами H и L в индексе обозначены соответственно высокотемпературная и низкотемпературная разновидности той или иной фазы; температуры фазовых переходов указаны в °С.Именно образующийся в клинкере b-ортосиликат гидратируется за 28 суток, обеспечивая твердение цемента. Остальные же разновидности очень слабо реагируют с водой, и твердения не могут вызвать [2]. Поэтому при спекании клинкера технологический процесс ведут так, чтобы не допустить образования ни a-, ни g-ортосиликатов. Если вовремя не остановить фазовые переходы, клинкер рассыплется в порошок, который твердеть практически не будет. Правда, некоторые примеси, всегда присутствующие в клинкере, способствуют “замораживанию” b-ортосиликата, необходимого для получения цементного камня [3].Сюрприз лежалого шлака
Самораспадающийся шлак, в котором содержится до 90% ортосиликата кальция - и почти весь он в g-форме, - охлаждается бесконтрольно. Из ковша расплавленный шлак выливают на площадку распада, где он образует огромные, раскаленные докрасна, глыбы. Остывая, они становятся оливковыми, вся поверхность их вздувается, и начинают брызгать фонтанчики тонкого белого порошка, еще очень горячего. Через несколько минут глыбы превращаются в горки белого или слегка сероватого порошка. Но он, к сожалению, не твердеет от воды.
Рассыпавшийся шлак с площадки распада транспортируют в отвал. Трудно описать, сколько вреда приносит хранение этого пылевидного шлака! Ветер разносит его по округе, отчего у местного населения возникают заболевания легких и глаз. Смытая дождями и талыми водами шлаковая пыль загрязняет почву и водоемы, растворимые компоненты проникают в грунтовые воды, а затем в родники и колодцы…
Но вот оказывается, что, пролежав в отвале примерно полгода, толща рассыпавшегося шлака покрывается твердой коркой толщиной 10-15 см. Может, она образовалась за счет длительного взаимодействия шлака с водой и медленная реакция гидратации все же делает свое дело? Местное население Чусового и окрестных населенных пунктов довольно давно обнаружило, что, если разбить корку, под ней окажется рыхлый шлак, но уже не безразличный к действию воды, а взаимодействующий с ней точно так же, как обычный портландцемент - быстро и очень эффективно. Жители вместо него и используют такой лежалый шлак для строительных нужд: штукатурят стены домов и квартир, бетонируют дорожки усадеб, готовят кладочные растворы и т.д. [4].
Лежалый шлак не только быстро твердеет, но еще и оказывается значительно устойчивее портландцемента к намоканию. Дело в том, что прочность всех (за редким исключением) намокших материалов снижается: керамического кирпича - примерно на 15%, силикатного - на 30-35. Оказалось, что водостойкость (или коэффициент размягчения, который выражают отношением прочности насыщенного водой материала к прочности сухого) затвердевшего самораспадающегося шлака составляет величину 0.9, тогда как для портландцемента она обычно равна 0.8-0.83.
Очень уж заманчиво вместо того, чтобы вывозить в отвал такой шлак, использовать его в качестве цемента. Прочного, водостойкого, к тому же - белого! Но ждать полгода… Да еще с не совсем предсказуемым результатом: а какова будет марка самородного цемента и другие важные его свойства (сроки схватывания, время твердения, усадка или расширение при твердении)?
Но самый трудный вопрос, почему же затворенный водой шлак неожиданно приобретает способность твердеть? Ведь переход из g-формы ортосиликата в b-форму термодинамически запрещен! Не сказывается ли влияние чего-либо сопутствующего?
Полезные спутники
Переходные элементы, или d-элементы (например скандий, титан, ванадий, хром, марганец, железо, кобальт, никель, медь и цинк), как известно, легко образуют комплексные соединения, которые могут служить катализаторами разных реакций, способствовать кристаллизации аморфных фаз, в частности, силикатных стекол.
При получении портландцементного клинкера некоторые переходные элементы в небольших количествах (доли процента) присутствуют в составе сырьевой смеси и обеспечивают ускоренное образование минеральных кристаллогидратов. А это повышает активность портландцемента, прочность затвердевшего цементного камня.
В шлаке тоже содержатся переходные элементы: титан (до 1%), хром и железо (примерно по 0.5%), ванадий (его количество в феррованадиевом шлаке, например, колеблется от 0.1 до 2% и более). Эти элементы не образуют собственных минералов, а входят в состав ортосиликатов кальция, замещая некоторые атомы кальция в кристаллической решетке. В результате образуются так называемые твердые растворы, хорошо знакомые геологам и минералогам. В ортосиликате кальция подобное замещение атомами железа стабилизирует способную к гидратации b-форму.
Как же могут повлиять переходные элементы, входящие в состав самораспадающегося шлака, на его свойства? Ведь при остывании ортосиликат кальция бурно переходит в нетвердеющую g-форму, а из нее b-разновидность возникнуть не может. Тем не менее рентгеноструктурный анализ показывает, что через полгода в шлаке количество g-ортосиликата уменьшается в 10 раз, а вместо него непонятно откуда появляется (столько же, сколько прежде было g-модификации) b-форма. Мог ли осуществиться вопреки законам термодинамики переход кристаллической g-фазы в b-фазу, или она возникла по каким-либо другим причинам? А что если минерал, который считается g-ортосиликатом кальция, на самом деле представляет собой твердый раствор какого-то другого минерала в ортосиликате кальция? Твердые растворы ведь могут распадаться, образуя новые фазы. Возможно, в шлаке именно это и происходит, а потому образуется новый минерал и b-ортосиликат кальция.
Шлак под микроскопом
Многие пытались найти способ утилизации самораспадающегося шлака. М.М. Сычеву (в металлургической отрасли он - один из крупнейших российских исследователей вяжущих материалов) удалось добиться твердения такого шлака, добавив к нему 2-4% гипса и подвергнув смесь автоклавированию, т. е. тепловой обработке в атмосфере насыщенного водяного пара при давлении 0.8-1.2 МПа. По данным Р.Ф. Руновой из Киевского инженерно-строительного института, можно получать прочные изделия из некоторых гидросиликатов кальция несколько иначе: прессованием при высоком давлении самораспадающегося шлака с небольшим количеством воды (до 10%). Если превышается некий предел давления (примерно 4-5 МПа), то прессование даже без воды скачком переводит порошок в твердое тело высокой прочности. Правда, вода в нем присутствует в кристаллизационной форме.
Все эти превращения в конечном счете связаны с фазовыми переходами в системе. Но какие именно переходы осуществляются при активации гидравлически неактивных веществ? Нельзя исключить, что присутствующий в Чусовском шлаке ванадий влияет на свойства ортосиликата кальция.
Для проверки этого предположения заводские технологи специально получили 10 проб шлака, отличающихся содержанием ванадия. Затем их исследовали в поляризационном микроскопе, чтобы определить угол погасания (как известно, это важная характеристика минералов) образовавшихся кристалликов ортосиликата кальция. Выяснилось, что с увеличением содержания ванадия в ортосиликате угол погасания увеличивается (рис. 2). Значит, изменяется структура кристалла. Возможно, внедрением атомов ванадия в кристаллическую решетку g-ортосиликата и объясняется появление у него способности к гидратационному твердению.
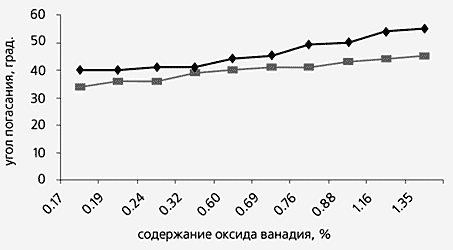
Рис. 2. Корреляция между содержанием ванадия в шлаке и углом погасания
кристаллов ортосиликата кальция в b-форме (цветная кривая) и g-модификации.Это предположение было проверено экспериментально на образцах заводского шлака - свежего, только что распавшегося, и лежалого, пробывшего год в отвале. Контролем служили пробы g-ортосиликата кальция, синтезированного в лаборатории - чистого и с добавками оксидов ванадия. Во все образцы добавляли дистиллированную воду (30%) и прессовали под давлением 20 МПа. Естественно, что изучали и прочность затвердевших составов через 28 суток, затем через три месяца, полгода и год.
В результате удалось подтвердить, что свежий шлак с водой практически не реагирует. В поле зрения микроскопа было видно, что лишь очень незначительная часть поверхности его зерен обрастает едва заметной бахромой гидратных новообразований (рис.3). Но даже после года твердения эти образцы не превращались в прочное твердое тело.

Рис. 3. Зерна шлака в поле зрения электронного микроскопа
Бахрома гидратных новообразований видна в виде мелких зазубрин по краям зерна (увел. в 200 раз).
Лежалый шлак ведет себя по-другому. Через семь суток появляются новообразования в виде кристалликов гидросиликата кальция (он всегда возникает при твердении портландцемента и довольно хорошо изучен), а к концу шестого месяца по размерам становятся больше контрольных зерен синтетического ортосиликата (рис. 4). Прочность образцов через 28 суток составляла около 25 МПа. В контрольных препаратах, содержащих не менее 0.7% ванадия, кристаллогидраты образовывались так же быстро и не отличались от тех, что обычно возникают при твердении цемента.
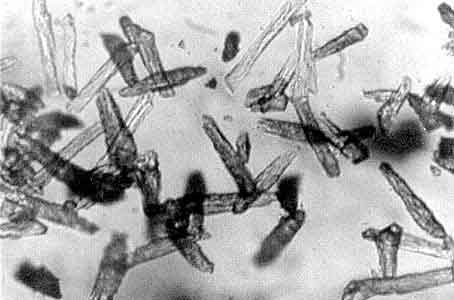
Рис. 4. Кристаллы синтетического гидросиликата кальция (увел. в 200 раз).
Активизированный, т. е. содержащий ванадий, шлак был использован в дальнейшем вместо цемента для приготовления бетона. В нем, судя по результатам электронной микроскопии, присутствовали такие же кристаллики гидросиликата, что и в твердеющем цементе (рис.5).

Рис. 5. Кристаллы гидросиликата кальция в образце бетона,
для приготовления которого использовался шлак, содержащий ванадий.Таким образом, в экспериментах удалось доказать превращение нетвердеющего ортосиликата кальция в твердеющий. Но действительно ли это связано с фазовым переходом g-модификации в b-форму, еще неизвестно. А может быть, твердый раствор в присутствии ванадия распадается на b-ортосиликат и какой-то, еще не установленный минерал, также способный к гидратации? Пока кандидата на такой новый минерал не найдено. Остается допустить, что гипотетическое превращение все же существует.
Для чего все это нужно
На первый взгляд не очень-то целесообразно получать из шлака вяжущий материал, прочность которого ниже, чем у цемента самой низкой марки. Нет! Оказывается, низкомарочные вяжущие материалы давно и настоятельно необходимы строительству. Ведь на приготовление их растворов сегодня расходуется дорогостоящий портландцемент. А из самораспадающегося шлака получается вяжущее вещество как раз низкомарочное, наиболее подходящее для штукатурных и кладочных строительных растворов. Да к тому же с более высокой, чем у портландцемента, водостойкостью.
Кстати, марки рядового строительного гипса тоже невысоки, кроме того, их водостойкость очень низка. А вяжущий материал из шлака и прочнее гипса, и, как сказано, имеет более высокую водостойкость, и медленнее схватывается. И к тому же он белого цвета.
Если считать, что гипотетическое превращение все же существует, то нужно искать способы его ускорения. Ждать полгода, пока произойдет желанный переход, явно нетехнологично. Здесь уже упоминалось о так называемой сульфатной активации нетвердеющего самораспадающегося шлака добавлением гипса с последующим автоклавированием.
Но вот что интересно. На том производстве, где образуется такой шлак, есть сернокислый сток, в котором концентрация серной кислоты достигает 6% и более. Его нельзя сливать в канализацию, он отравит речную воду. Поэтому сток нейтрализуют известью. В результате появляется вторичный гипс, который, как и шлак, отправляют в отвалы - многотоннажные экологически опасные толщи. Так вот, сернокислотный сток можно использовать вместо воды при формовании изделий прямо из шлака, образцы формовать при давлении 30-40 МПа, а потом подвергнуть их пропариванию, т.е. тепловой обработке при влажности близкой к 100%, но при атмосферном давлении. Эта технология используется при изготовлении бетонных и железобетонных конструкций и таким же способом в экспериментах был получен водостойкий безобжиговый белый кирпич марок “100” и “150”.
Итак, из нетвердеющего самораспадающегося шлака феррованадиевого производства можно получать строительные материалы вроде кирпича и одновременно утилизировать не только сам шлак, но и еще один необычайно опасный вид отходов - сернокислотный сток. Остается осуществить это практическое приложение теории.
Работа поддержана Российским фондом фундаментальных исследований. Проект 01-03-96495-р2001урал Р.
Литература
1. Горшков В.С., Александров С.Е., Иващенко С.И., Горшкова И.В. Комплексная переработка и использование металлургических шлаков в строительстве. М., 1985.
2. Горшков В.С. // Журн. прикл. химии. 1966. Т.39. ?2. С.448-451.
3. Гатт В., Нерс Р. Фазовый состав портландцементного клинкера // Тезисы VI Международного конгресса по химии цемента. 1976. Т.1. С.78-88.
4. Баталин Б.С., Беляева И.В., Макарова Л.Е. О взаимосвязи между фазовым составом феррованадиевого самораспадающегося шлака и его вяжущими свойствами // Журн. прикл. химии. 1996. Т.69. Вып.1. С.162-164.