№10, 2003 г.
© Н.Г. Левицкая, А.А. Каменский
Регуляторные пептиды
Н.Г. Левицкая, А.А. Каменский
Наталья Григорьевна Левицкая, к.б.н., научный сотрудник лаборатории молекулярных основ регуляции поведения
Андрей Александрович Каменский, д.б.н., зам. зав. каф. физиологии человека и животных биофака МГУ,
Института молекулярной генетики РАН.
зав. лаб. молекулярных основ регуляции поведения того же института.
Ровно 20 лет назад, в 1983 г., в “Природе” появилась статья, посвященная нейропептидам. Тогда об удивительных свойствах этих веществ знали еще немного, а об их фармакологическом применении можно было только мечтать. Сегодня мы расскажем о новом нейротропном лекарстве, созданном отечественными специалистами на основе регуляторного пептида.
Любому многоклеточному организму необходимы системы, превращающие миллиарды самых разнообразных по строению и функции клеток в единое гармоничное целое. Всегда считалось, что таких регуляторных систем три: иммунная, которая оберегает организм от чужеродных агентов, в частности болезнетворных; нервная, реагирующая на изменения окружающей среды и обеспечивающая быстрые ответные реакции (благодаря чему мы и выживаем в постоянно меняющемся мире); эндокринная, которая работает медленнее нервной, зато ее эффективность сохраняется достаточно долго.
В последние годы становится все более очевидным, что эти системы в сущности представляют собой единое целое, и доказательств тому множество. Например, показано, что отрицательные эмоции, приводящие к депрессии, значительно снижают иммунитет, а положительные, напротив, служат его стимулятором. Описаны и документально подтверждены случаи, когда неожиданное радостное известие (например, нашелся ребенок, пропавший во время войны) помогало больным избавиться от онкологических заболеваний. Еще теснее связаны нервная и эндокринная системы. Сегодня известно, что весь мозг (и особенно гипоталамус) - это эндокринный орган. В нейронах ядер гипоталамуса синтезируются гормоны - вазопрессин и окситоцин, там же образуется целый набор коротких пептидов - либеринов и статинов, управляющих работой всей эндокринной системы.
Одним из главных звеньев, объединяющих все три системы в единую, служат регуляторные пептиды. Открыли их относительно недавно, около 50 лет назад, и до настоящего времени активно исследуют. Эти небольшие белковые молекулы, состоящие из аминокислотных остатков (обычно от двух до 50), вырабатываются практически во всех органах. В одних случаях они выделяются из синаптического окончания и действуют на одну постсинаптическую клетку, выполняя функцию медиатора; в других - оказывают влияние на небольшое число клеток, окружающих родительскую молекулу, т.е. служат модуляторами, в третьих - с током крови достигают отдаленных участков организма и работают как гормоны. Интересно, что один и тот же пептид может выступать во всех трех ролях.
Область биологической активности пептидов чрезвычайно широка (табл.). Они влияют на состояние сердечно-сосудистой, иммунной, половой, эндокринной, пищеварительной и других систем, изменяют энергетический обмен в организме, но особенно эффективны в регуляции работы центральной нервной системы. Одна из наиболее характерных черт - их полифункциональность (один и тот же пептид может модулировать работу многих систем организма). Более того, их фрагменты, возникающие при распаде в организме, могут обладать собственной физиологической активностью.
Большинство регуляторных пептидов образуется из физиологически неактивных белков-предшественников с помощью специальных ферментов, протеаз, которые в нужный момент “вырезают” необходимую аминокислотную последовательность. Иногда из одного предшественника появляется целая группа пептидов, необходимая для успешного приспособления различных систем организма к определенным изменениям окружающей среды. Так, из белка про-опиомеланокортина (265 аминокислотных остатков), который синтезируется в клетках гипоталамуса и в других участках мозга, возникает семейство коротких пептидов: адренокортикотропный гормон (АКТГ), способствующий выбросу гормонов из надпочечников; меланоцитстимулирующие гормоны (a-, b- и g-МСГ), регулирующие окраску кожи и волосяного покрова; b-эндорфин - пептид морфиноподобного действия; b-липотропин - регулятор жирового обмена и др. Сам белок-предшественник не обладает активностью входящих в его структуру пептидов, но при необходимости из него можно быстро (значительно быстрее, чем путем рибосомального синтеза) получить необходимые организму продукты. Например, в случае опасной ситуации система анализаторов (зрительного, слухового, обонятельного и т.п.) сообщает в мозг о происходящем, и в нейронах гипоталамуса из белка “вырезаются” АКТГ и b-эндорфин. Так организм получает стимулятор обмена и обезболивающее средство, что помогает ему в борьбе с вероятным врагом.
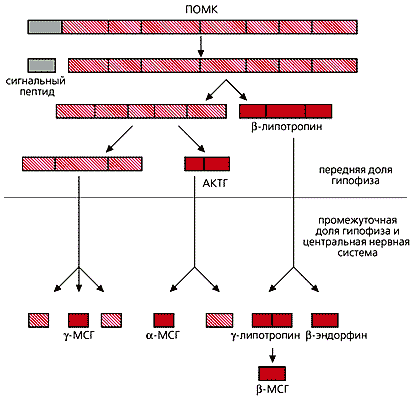
Схема образования регуляторных пептидов
из неактивного белка-предшественника про-опиомеланокортина (ПОМК).В настоящее время АКТГ, МСГ, их фрагменты и синтетические аналоги объединяют термином “меланокортины”. Еще в 70-е годы прошлого столетия голландский исследователь Дэвид де Вид установил, что АКТГ не только усиливает синтез гормонов в клетках коры надпочечников, но и непосредственно влияет на мозг экспериментальных животных, стимулируя внимание и память. Дальнейшие исследования показали, что таким ноотропным действием обладает не только целая молекула гормона, но и его фрагменты. Наиболее эффективным из них оказался пептид из семи аминокислот, АКТГ4-10, занимающий в молекуле положение с 4-го по 10-е, а самый короткий фрагмент, сохраняющий активность целой молекулы гормона, - пептид АКТГ4-7. Выяснилось, что меланокортины ускоряют восстановление поврежденных нервов и созревание нервно-мышечной системы, а также оказывают противовоспалительное и жаропонижающее действие; влияют на болевую чувствительность; регулируют работу сердечно-сосудистой системы; моделируют половое поведение; обладают антиопиоидной активностью; снижают потребление пищи и массу тела.

Аминокислотные последовательности природных и синтетических меланокортинов.
Такой широкий спектр свойств меланокортинов предполагал использовать их в качестве лекарственных препаратов при самых различных заболеваниях. Однако здесь серьезным препятствием оставалась малая продолжительность эффектов природных соединений, не обладающих эндокринной активностью. Это связано с быстрым распадом пептидов в организме под действием ферментов. Для создания лекарств на основе меланокортинов необходимо было разработать их синтетические аналоги с природной активностью пептидов, но с высокой устойчивостью к действию протеаз. Зарубежные фармакологи попытались защитить регуляторный пептид, включая в его состав неприродные
D-изомеры или другие вставки, не встречающиеся в белках живых организмов. Однако такой путь пролонгации эффектов нельзя признать удачным. Ведь, по некоторым сведениям, именно D-изомеры аминокислот, накапливающиеся в стареющем организме, могут привести к развитию онкологических заболеваний. Так или иначе, но ни один из синтетических фрагментов АКТГ, созданных за рубежом, не прошел фармакологических испытаний. Единственный синтетический пептид этого класса, широко применяемый в медицине, разработан химиками из Института молекулярной генетики РАН под руководством М.Ф. Мясоедова и биологами кафедры физиологии человека и животных биологического факультета МГУ под руководством И.П. Ашмарина.
Основой для создания нового лекарства стал фрагмент АКТГ4-10, сохраняющий ноотропную активность целой молекулы гормона. Как показали исследования, этот фрагмент не действует на кору надпочечников, поскольку он не связывается с гормональным рецептором на клетках надпочечников. Это давало принципиальную возможность использовать АКТГ4-10, лишенный гормональных (в данном случае побочных) эффектов, как стимулятор внимания и памяти. Однако длительность эффектов природного пептида очень мала (в наших экспериментах на крысах она составляет 30 мин). Кроме того, его необходимо вводить в кровь, так как в желудке он очень быстро разрушается пепсином и соляной кислотой. Вот тогда-то исследователи из Института молекулярной генетики РАН поставили перед собой цель разработать такой искусственный аналог, который был бы эффективным и длительным стимулятором функций мозга. Было замечено, что к действию протеолитических ферментов устойчивы пептиды, обогащенные аминокислотными остатками пролина. Возникла идея защитить фрагмент АКТГ путем ввода в структуру его аналога остатков пролина. После испытания нескольких десятков синтетических аналогов отобрали пептид, в котором к природному фрагменту АКТГ4-7 присоединили три аминокислотных остатка (пролил-глицил-пролин), увеличивающие его протеолитическую устойчивость. На основе этого пептида и было разработано лекарство, названное семаксом. Продолжительность его действия превышает 20 ч (т.е. около суток), а эффективность столь же высока, как и у природных фрагментов АКТГ. Достаточно ввести крысам по пять миллионных долей грамма препарата, и у них на сутки возрастет способность к обучению.
Однако тут же возникла следующая проблема: как вводить семакс в организм человека? Таблетки не годятся, поскольку в желудке большую часть даже защищенного пептида разрушат ферменты, которые продолжат свою работу и в крови, а до мозга дойдет слишком мало препарата. Конечно, проще всего вводить лекарство внутримышечно или внутривенно, что практически весьма неудобно. Кроме того, вспомним, что изначально семакс создавался для людей определенных профессий (авиадиспетчеров и операторов АЭС, бойцов горноспасательных служб, спасателей МЧС, летчиков). Большинство из них работают в условиях, не пригодных для стерильных инъекций. Тогда в литературе появились публикации о способности некоторых пептидов хорошо проникать в кровь из полости носа. Причем молекулы веществ могли быть гораздо больше семакса. Многие сотни экспериментов на крысах показали, что и семакс весьма эффективно можно вводить человеку таким не вызывающим неприятных ощущений способом, просто закапывая в нос. Кстати сказать, механизмы интраназального проникновения веществ в мозг - предмет для отдельного разговора. Это очень интересная физиологическая проблема, имеющая большое прикладное значение.
После того как создатели семакса разобрались со способом его введения в организм, приступили к рутинным, но абсолютно необходимым фармакологическим экспериментам на предмет возможных побочных эффектов (мутагенных, тератогенных, канцерогенных и т.д.). Исследования продолжались несколько лет, а затем начались первые клинические испытания (надо сказать, что мы задолго до этого проверяли семакс на себе, регистрируя при этом параметры умственной работоспособности и вегетативные показатели: частоту сердечных сокращений, артериальное давление, температуру тела). Уже после первой стадии клинических испытаний семакс стали широко применять. В 2002 г. через аптечную сеть продали около 200 тыс. флаконов препарата.
Для чего же сегодня используют семакс? Сразу же хочется ответить на самый распространенный вопрос: делает ли семакс человека умнее? Нет. Не делает. Безграмотный человек, не читавший Н.В. Гоголя, не сможет вспомнить что-либо ни про Хлестакова, ни про Вакулу. Семакс помогает клеткам мозга выживать при гипоксии, т. е. улучшает работоспособность клеток при недостатке кислорода или глюкозы. Он усиливает селективное внимание и консолидацию памятного следа, т. е. человек более четко выделяет наиболее важные из действующих на него в данный момент стимулов, лучше их воспринимает, а затем эта информация надежнее фиксируется и хранится до тех пор, пока она не потребуется. Но семакс не только стимулятор обучения. Его можно и нужно применять и для коррекции ряда патологических состояний человека, например для улучшения работы мозга после глубокого наркоза, черепно-мозговых травм, в постреанимационном периоде. Высокоэффективен он и для людей, перенесших инсульт. Так, лечение семаксом в течение пяти дней позволяет значительно снизить число смертных случаев и ускорить восстановление нарушенных неврологических функций у больных с инсультами различной степени тяжести. Правда, в этом случае необходимы повышенные дозы препарата. Кроме того, важно не упустить время и начать лечение в пределах шестичасового интервала после нарушения мозгового кровообращения. В последнее время показана также высокая активность семакса при заболеваниях зрительного нерва.
И хотя сегодня семакс можно купить в аптеке, исследования физиологических эффектов и механизмов его действия продолжаются. На кафедре физиологии человека и животных биологического факультета МГУ работа идет в нескольких направлениях. Прежде всего необходимо было понять, что определяет длительность эффектов препарата. Протеолитический распад семакса (как и природного фрагмента АКТГ4-10) начинается с отщепления N-концевой аминокислоты и приводит к образованию гексапептида. Если же гексапептид из АКТГ4-10 очень быстро разрушается дальше, то синтетический аналог существует значительно дольше. Точно так же ведут себя пентапептиды.
Схема Т-образного лабиринта. Однако доказательства долгой жизни фрагментов семакса еще не объясняли большую продолжительность их эффектов. Мы проверяли биологическую активность всех пептидов, как природных, так и синтетических (от полного фрагмента до тетрапептида), изучая их влияние на скорость обучения белых крыс. В течение четырех дней животных учили находить корм в лабиринте. Ежедневно каждую крысу помещали в лабиринт пять раз. За 15 мин до сеанса вводили исследуемый пептид, а контрольным животным - дистиллированную воду. Критерием обученности служило число выполненных реакций в день, т.е. сколько раз крыса находила корм в лабиринте. Как показали результаты экспериментов, если активности АКТГ4-10 и семакса не отличались, то действие продуктов их распада было диаметрально противоположным. Так, отщепление одной аминокислоты от природного пептида резко снижало активность (число выполненных реакций превышало контрольные значения только на четвертый день обучения), а в случае семакса, напротив, она увеличивалась (т.е. опытные крысы обучались лучше контрольных). Лишь удаление трех аминокислотных остатков приводило к полной потере активности - скорость обучения в группе крыс, получавших тетрапептид, не отличается от контроля. Значит, большую продолжительность действия семакса определяют большая устойчивость и активность в организме их фрагментов.
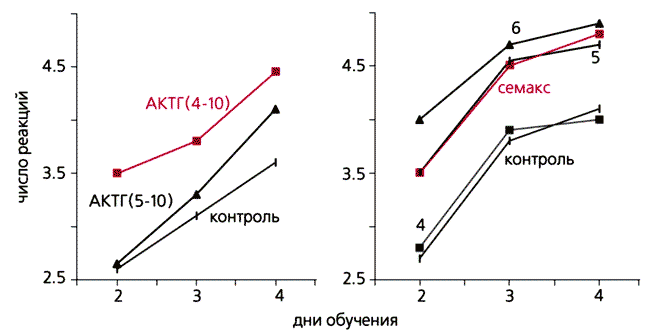
Влияние АКТГ4-10, семакса и их фрагментов на обучение белых крыс в лабиринте.
Фрагменты семакса: 6 - гексапептид, 5 - пентапептид и 4 - тетрапептид.На следующем этапе проверялись нейропротекторные эффекты семакса, т. е. его защитное действие при повреждениях нервной системы. В качестве повреждающего фактора использовали нейротоксин, который вызывает гибель нейронов мозга, содержащих дофамин (именно эти нейроны страдают у человека при болезни Паркинсона). У белых крыс такой нейротоксин изменяет поведение, в том числе снижает двигательную активность. Семакс, введенный крысам интраназально после нейротоксина, снимает отрицательные последствия, т. е. поведение животных не отличается от контроля.
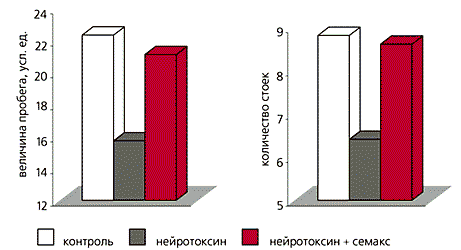
Защитное действие семакса на фоне нарушений поведения животных,
вызванных введением нейротоксина.Для изучения влияния семакса на развитие нервной системы новорожденным крысятам в течение второй и третьей недель жизни ежедневно вводили препарат (контрольным животным - воду), а затем два месяца наблюдали за их поведением. Взрослые крысы, получавшие в раннем возрасте семакс, отличались от контрольных более высокой исследовательской активностью и сниженной тревожностью. Такое поведение сохранялось даже через 30 дней после последнего введения пептида. Столь долговременное влияние семакса свидетельствует о его эффективности в неонатальный период.
Известно, что природные меланокортины ослабляют болевую чувствительность человека и животных. Мы проверили эту способность на белых крысах. В опытах использовали тест сдавливания задней конечности. Болевым раздражителем служило равномерно нарастающее давление на задние лапы крысы. В момент возникновения боли животное, естественно, отдергивает лапу. Уже через 15 мин после введения семакса болевой порог увеличивается - крысы опытной группы выдерживают большее давление, чем контрольные. Следовательно, семакс снижает болевую чувствительность крыс.
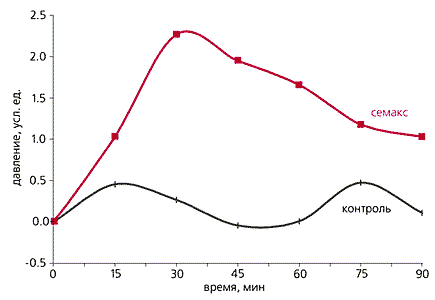
Влияние семакса на болевую чувствительность белых крыс.
Из литературы известно, что меланокортины, обладая собственной анальгетической активностью, при совместном введении с опиоидами (веществами с морфиноподобным действием) уменьшают их противоболевое действие. Подобный эффект мы продемонстрировали и на семаксе при одновременном введении его с морфином. Антиопиоидные свойства семакса, как и других меланокортинов, вызывают большой интерес, так как свидетельствуют о их взаимодействии с опиоидной системой организма. Такой эффект пептидов этого класса говорит о возможном влиянии меланокортинов и их аналогов (в частности семакса) на развитие наркотической зависимости.
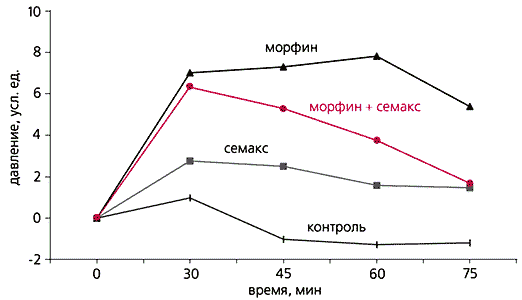
Ослабление анальгетического эффекта морфина при совместном действии с семаксом.
Итак, сегодня нет никаких сомнений, что семакс улучшает обучение и память, оказывает защитное действие при повреждениях нервной системы, влияет на процессы развития нервной системы, вызывает снижение болевой чувствительности и обладает антиопиоидной активностью. Широкий спектр активности синтетических пептидов открывает возможности для создания и использования в медицине лекарственных препаратов. Результаты, полученные при исследовании физиологических эффектов природных и синтетических меланокортинов, еще раз подтверждают, что регуляторные пептиды - это своеобразные химические интеграторы, координирующие работу всех управляющих систем организма - нервной, эндокринной и иммунной.