№11, 2003 г.
60 лет Институту кристаллографии им.А.В.Шубникова РАН
© В.И.СимоновФизическими свойствами кристаллов
можно управлятьВ.И. Симонов
Валентин Иванович Симонов, д. ф.-м.н., проф., гл.н.с. лаборатории рентгеноструктурного анализа.
Кристаллы - это преобразователи одного вида энергии в другой, созданные самой природой. Если механически сжать пьезокристалл, на его поверхности появится электрический заряд. Если воздействовать на такой кристалл переменным электрическим полем, кристалл начнет вибрировать, генерируя ультразвук определенной частоты. Освещенный лампой накачки лазерный кристалл становится источником когерентного лазерного луча. Кристаллические материалы с ионной проводимостью лежат в основе миниатюрных источников тока. А если к этому добавить полупроводники, сегнетоэлектрики, магнитные и другие кристаллические материалы с особыми физическими свойствами, то роль, которую играют кристаллы в нашей жизни, станет очевидной. Развиваясь, техника выдвигает новые, все более жесткие требования к их физическим свойствам.
Как достичь цели
Часто используемый при поиске и синтезе новых кристаллических материалов метод проб и ошибок весьма затратен. Чтобы перейти к целенаправленному получению новых кристаллов, необходимо знать, как связаны между собой химический состав, атомная структура и физические свойства кристаллов. Центральное место в этой последовательности занимает атомное строение кристаллов, которое расшифровывается методами дифракции рентгеновских лучей, нейтронов или электронов *.
* Подробнее о современных методах определения структуры вещества см.: Структурный анализ сегодня // Природа. 1997. №7. С.31-78.Кристалл - периодическая трехмерная структура. Современная структурная кристаллография позволяет определять симметрию кристалла (принадлежность его к одной из 230 федоровских групп), размеры и форму его элементарной ячейки, координаты базисных атомов структуры и параметры теплового движения атомов с учетом анизотропии и ангармонизма тепловых колебаний. Установить закономерности в ряду состав-структура-свойства можно на основе синтеза, структурных и физических исследований серий кристаллов, отличающихся химическим составом, но кристаллизующихся в одном структурном типе. Изучение таких рядов соединений с изоморфными замещениями позволяет выявить структурную обусловленность интересующих исследователя физических свойств. Существует и иной путь решения задачи. Если в исследуемом кристалле при вариации температуры или наложении гидростатического давления происходят фазовые переходы, то фактически до и после перехода мы имеем кристаллы одного состава, но разного строения с отличающимися физическими свойствами. Сопоставление изменений структурных параметров и физических свойств дает возможность надежно устанавливать соответствующие корреляции.Понимание связей состав-структура-свойства открывает путь управления физическими характеристиками кристаллов с помощью изоморфных замещений. Области возможного изменения свойств всегда ограничены, но такие вариации могут перекрывать интервалы в несколько порядков величины.
Носитель тока - ион
Имеются семейства кристаллов, в которых, в отличие от металлов, проводимость обусловлена движением не электронов, а ионов, способных перемещаться по кристаллу благодаря наличию в его структуре каналов. Подобные кристаллы с высокой проводимостью s>1·10–3 Ом–1·см–1) относят к суперионным материалам или твердым электролитам. Можно утверждать, что наряду с электроникой развивается ее младшая сестра - ионика твердого тела [1]. Суперионики занимают все более заметное место в физике твердого тела и материаловедении. Так, на основе нестехиометрических фторидов M1–x+2Rx+3F2+x–1 со структурой флюорита CaF2 созданы применяемые на химических предприятиях датчики, фиксирующие появление в атмосфере следов фтора. В этих датчиках под действием напряжения источника питания “собственные” ионы фтора собираются у электрода и ток отсутствует; если же фтор попадает в датчик из окружающей среды, то проводимость восстанавливается. Суперионики позволяют создать конденсаторы гигантской емкости, которая обусловлена атомно-малыми расстояниями между обкладками. Промышленность освоила производства конденсаторов фарадной емкости на их основе. Пальму первенства в практическом использовании, безусловно, держат миниатюрные источники электропитания, в которых суперионики служат основной составляющей. По запасам количества электричества на единицу веса лидируют батарейки и аккумуляторы на основе супериоников с проводимостью по ионам лития. Если вы ставите в электронные ручные часы новую крохотную литиевую батарейку, то на ближайшие два-три года у вас не возникает проблемы с необходимостью ее замены. Миниатюрные источники тока используются на каждом шагу - от детских игрушек до портативных вычислительных машин и мобильных телефонов. По оценкам специалистов, мировая сумма продаж таких источников тока достигает миллиардов долларов США в месяц.
В основе атомной структуры кристаллов с высокой ионной проводимостью обычно лежит прочный и ажурный трехмерный каркас, пронизываемый каналами различной формы и сечения. В таких каналах статистически локализуются ионы, которые под действием электрического поля приходят в движение и транспортируют заряды. В свое время в Институте кристаллографии были синтезированы суперионные соединения с проводимостью по литию нового структурного типа [2] - кристаллы составов Li3Sc2(PO4)3 и Li3Fe2(PO4)3. В этих соединениях при разных температурах происходят два фазовых перехода, причем суперионной является высокотемпературная фаза. У выращенных монокристаллов была расшифрована атомная структура (рентгеновскими и нейтронографическими методами) и установлены проводящие свойства. Ионная проводимость по литию в них при комнатной температуре оказалась равной 1·10–5 Ом–1·см–1, а в суперионном состоянии - 1.8·10–2 Ом–1·см–1. Модель атомной структуры кристалла Li3Sc2(PO4)3 представлена на рис.1.
Трехмерный каркас структуры построен из октаэдров [ScO6] и тетраэдров [PO4], соединенных через общие кислородные вершины. В каналах этого каркаса располагаются ионы лития. Если симметрия низкотемпературных фаз этих кристаллов моноклинная и характеризуется федоровской группой симметрии P21/n, то при переходе в суперионную фазу каркас структуры симметризуется до ромбического, и структура реализуется в рамках группы симметрии Pcan. Имеющиеся в элементарной ячейке кристалла 12 ионов лития в суперионной фазе статистически размещаются по трем кристаллографически независимым позициям, суммарная кратность которых равна 24 (иначе говоря, половина из возможных положений не занята). Поскольку литий слабо рассеивает рентгеновские лучи, пришлось перейти к уточнению заселенностей литием своих позиций по нейтронографическим дифракционным данным [3]. Благодаря последним была установлена существенно различная степень заселенности литием своих кристаллографических позиций, что и служит причиной анизотропии проводимости по ионам лития в этих соединениях. Близок по механизму проводимости к ним суперионный проводник по натрию Na4Ti(PO4)2O, где электропроводность в суперионной фазе достигает 2.5·10–2 Ом–1·см–1.Рис.1. Модель структуры Li3Sc2(PO4)3. Ажурный трехмерный каркас образован [ScO6]-октаэдрами и [PO4]-тетраэдрами. В каналах каркаса размещаются ионы лития (шарики).
Яркий пример твердых электролитов, в которых ионную проводимость можно путем изоморфных замещений целенаправленно изменять в сотни раз, дают соединения со структурой типа KTiO(PO4). На рис.2 представлена модель такой структуры. Каркас построен из [TiO6] октаэдров и [PO4] тетраэдров. В отличие от структуры Li3Sc2(PO4)3, в которой разрозненные октаэдры объединяются в каркас только тетраэдрами, в KTiO(PO4) сами октаэдры через общие кислородные вершины объединены в пронизывающие весь кристалл цепочки. Тетраэдры скрепляют эти цепочки уже в трехмерный каркас. В каналах винтообразной формы размещены ионы калия, которые и переносят ток. В этих соединениях калий можно частично или полностью заменить на натрий, таллий, рубидий или цезий. Однако резкое увеличение ионной проводимости достигается иными замещениями. В исходной структуре валентности атомов характеризуются следующими значениями: K+1Ti+4O–2(P+5O4–2). Как оказалось [4], если четырехвалентный титан частично заменить на пятивалентный ниобий, сохранив количество кислорода, для компенсации избыточной положительной валентности возникнет соответствующий дефицит ионов калияРис. 2. Модель структуры KTiO(PO4).
Цепочки из [TiO6]-октаэдров объединены [PO4]-тетраэдрами в каркас.
Катионы калия локализуются в каналах каркаса, заселяя свои позиции, показанные светлыми кружками, статистически.K1–x+1Ti1–x+4Nbx+5O–2(P+5O4–2).
При этом калий в каналах структуры рассредоточивается и занимает свои позиции статистически. Дефектность в заселенностях калием своих позиций обеспечивает возможность его движения по каналам. В твердом растворе, в котором 2 ат.% титана замещены ниобием K0.98Ti0.98Nb0.02O(PO4), электропроводность при фазовом переходе в суперионное состояние увеличивается на полтора порядка.
Световой луч взаимодействует с кристаллом
Лазерная техника, оптоэлектроника и другие разделы прикладного материаловедения нуждаются в кристаллических материалах с особыми оптическими характеристиками. Кристаллы с нелинейными оптическими свойствами используются для удвоения частоты лазерного излучения, для записи голограмм, для модуляции светового луча и передачи с его помощью огромных объемов информации без искажений на большие расстояния и т.д. Упомянутые выше твердые растворы со структурой KTiO(PO4) не только твердые электролиты, но и кристаллы с нелинейными оптическими характеристиками. Кристаллы KTiO(PO4) успешно используются для удвоения частоты лазерного излучения иттрий-алюминиевого граната с неодимом Y3Al5O12:Nd+3. При этом излучение с длиной волны l=1064 нм преобразуется в излучение с l=532 нм при эффективности до 85%. Если сравнить интенсивность второй гармоники от кристалла KTiOРО4 и от кристалла SiO2 при равных условиях, то выигрыш для первого будет примерно в 400 раз.
Ответ на вопрос о том, какие структурные характеристики отвечают за нелинейные свойства, дают исследования монокристаллов непрерывного ряда твердых растворов в системе KTiO(PO4)-KSnO(PO4) [5]. Когда степень замещения титана оловом возрастает, нелинейные характеристики материалов ухудшаются и интенсивность излучения второй гармоники падает - в кристалле KSnOPO4 она практически отсутствует. Рентгеноструктурные исследования монокристаллов KTi1–xSnxOPO4 с разным соотношением титана и олова позволили установить, что свойство нелинейности коррелирует с асимметрией положения атома катиона в октаэдрах [TiO6]. На рис.2 видны цепочки из Ti-октаэдров, в которых чередуются два кристаллографически независимых атома титана Ti(1) и Ti(2). Анализ межатомных расстояний титан-кислород показал, что одно расстояние Ti–O в каждом из октаэдров укороченное (сильная титанильная связь), напротив сильной связи находится удлиненная (ослабленная) связь, а четыре экваториальных связи Ti–O имеют средние значения. Таким образом вдоль цепочек чередуются укороченные и удлиненные связи. В кристалле KTiOPO4 чередующиеся длины связей равны: –O = 1.716 A = Ti(1)–1.985 A –O = = 1.736 A = Ti(2)–2.099 A –O=. Разности этих длин D(Ti–O) в одном и другом октаэдрах соответственно 0.269 A и 0.363 A.
При изоморфном вхождении олова в титановые октаэдры связи начинают постепенно выравниваться и в кристалле KSnOPO4 они становятся –O–1.978 A– –Sn(1)–1.975 A –O–1.961 A– –Sn(2)–1.957 A –O–, а их разности падают до 0.003 A и 0.004 A.
Такая симметризация связей оказывается губительной для нелинейности, и вторая гармоника излучения от кристаллов со 100% олова практически полностью исчезает. Итак, нелинейные характеристики твердых растворов K(Ti,Sn)OPO4 могут целенаправленно регулироваться путем изменения отношения количеств титана и олова в образце.
Еще одно семейство соединений с контролируемыми нелинейными характеристиками - твердые растворы ниобата стронция-бария (SrxBa1–x)Nb2O6. Эти кристаллы не только обладают оптическими нелинейными свойствами, но и являются пьезо- и пироэлектриками. Первое структурное определение монокристаллов состава (Sr0.73Ba0.27)Nb2O6 было выполнено еще в 1968 г., но исследования атомного строения таких кристаллов с различным содержанием стронция и бария продолжаются и в наши дни. Прецизионные структурные результаты [6] получены для твердых растворов с содержанием в соединениях (SrxBa1–x)Nb2O6 стронция х=0.33; 0.50; 0.61 и 0.75. Установлено, что твердые растворы с интересующей нас структурой (обеспечивающей упомянутые свойства) существуют только при содержании стронция в кристаллах в пределах 0.25<x<0.75. Из структурных исследований стали ясны причины этих ограничений. Данные твердые растворы кристаллизуются в рамках ацентричной тетрагональной группы симметрии P4bm. В элементарной ячейке кристалла объемом 613 A3 содержится пять формульных единиц состава (Sr,Ba)Nb2O6. Атомная модель структуры таких кристаллов представлена на рис.3. Два кристаллографически независимых сорта Nb-октаэдров - [Nb(1)O6] и [Nb(2)O6] - образуют каждый свои колонки, простирающиеся параллельно оси z - четверной оси симметрии кристалла. Октаэдры в колонки объединяют атомы O, каждый из которых с равной вероятностью заселяет одну из двух близко расположенных позиций. Колонки между собой соединены через общие кислородные вершины, занимающие фиксированные положения. Как видно из рисунка, структуру пронизывают сквозные каналы трех сортов. Минимальный диаметр - у каналов треугольного сечения, они всегда пусты. В средних каналах квадратного сечения локализуется только стронций. Барий размещается в самых широких каналах пятиугольного сечения, там же находится и часть стронция.
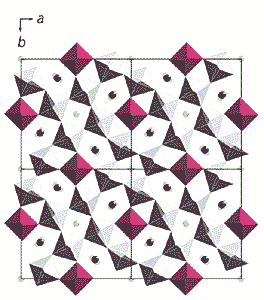
Рис. 3. Модель структуры (Sr,Ba)Nb2O6.
В каркасе из [NbO6]-октаэдров параллельно оси z (перпендикулярно плоскости рисунка) идут каналы трех типов. Каналы треугольного сечения пусты. В каналах квадратного сечения статистически размещен стронций. В самых широких каналах пятиугольного сечения статистически локализуется весь барий и частично стронций (эти позиции показаны кружками: темными - для бария и светлыми - для стронция).Суммарная кратность позиций в каналах двух типов равна шести, а, как сказано выше, атомов (Sr,Ba) на элементарную ячейку приходится всего пять. Структурные исследования показали, что при любом допустимом соотношении стронция и бария заселенность каналов всегда статистическая, а дефекты в форме вакансий присутствуют в квадратных и пятиугольных каналах. Именно эта дефектность служит причиной релаксорных свойств сегнетоэлектриков (SrxBa1–x)Nb2O6. При изменении количества стронция в кристалле от x=0.33 до x=0.75 позиции с кратностью, равной двум, в квадратных каналах заселяются в пределах 70.5-72.5%. Если весь стронций сосредоточен в квадратных каналах, для такой заселенности достаточно его количества на формульную единицу x=0.25, что и определяет нижнюю границу устойчивости данного типа структур. Остальной стронций размещается в широких каналах статистически, деля позиции с барием. Суммарная заселенность пятиугольных каналов барием и стронцием для всех исследованных структур лежит в пределах 84.0-89.1%. Позиции бария и стронция в этих каналах не совсем совпадают. Расстояние, на которое они пространственно разнесены, зависит от количества стронция. Особенно важно то, что изменение отношения бария и стронция сказывается на асимметрии положения атомов ниобия в своих октаэдрах, - это самым существенным образом влияет на нелинейные оптические характеристики. Как и в цепочках из Ti-октаэдров в кристаллах KTiOPO4, в цепочках из Nb-октаэдров ниобата стронция-бария чередуются короткие сильные и удлиненные слабые связи Nb–O. Разница в длинах этих связей максимальна при минимальном возможном содержании в кристалле стронция. При увеличении количества стронция различие в связях постепенно сокращается, что коррелирует с уменьшением параметра нелинейности соответствующих твердых растворов. В отличие от кристаллов KTiOPO4, в (SrBa)Nb2O6 для регулирования оптических свойств нет нужды вводить в структуру новые легирующие атомы, достаточно варьировать соотношение стронция и бария в образце.Старый знакомый - ниобат лития
Ниобат лития LiNbO3 - давно известный и широко применяемый в оптике и лазерной технике материал. При первых же структурных исследованиях в монокристаллах этого соединения было обнаружено существенное отклонение от стехиометрического состава [7] - содержание атомов Li и Nb различалось. Варьирование условий синтеза несколько меняло степень нарушения стехиометрии, но во всех случаях наблюдался избыток ниобия и дефицит лития. Лучшим качеством для оптических применений обладают кристаллы так называемого конгруэнтного состава, когда составы шихты и растущих монокристаллов одинаковы. Таковыми являются кристаллы, в которых избыток ниобия составляет примерно 1.5 ат.%. Для компенсации разности в валентностях ниобия Nb+5 и лития Li+1 недостаток лития при этом достигает 6.0 ат.%.
Структура ниобата лития, в основе которой лежит плотнейшая гексагональная упаковка из атомов кислорода, реализуется в пространственной группе симметрии R3c. Октаэдрические пустоты этой упаковки заселены упорядоченно на 1/3 ниобием, на 1/3 литием, последняя треть октаэдров остается пустой (рис.4). Авторы работы [7] показали, что избыточный ниобий замещает литий в его позициях и развернутую химическую формулу кристалла следует писать в общем виде (Li1–5xNbx}4x)NbO3 или конкретно (Li0.925Nb0.015}0.060)NbO3, где квадратом обозначены вакансии в позициях лития. Для придания устойчивости к мощному лазерному облучению кристаллы ниобата лития легируют такими элементами, как Mg, Zn, In, Sc и др. Сотрудники нашего института при исследовании зависимости оптических характеристик кристаллов LiNbO3:Zn (величины линейного электрооптического эффекта, фоторефракции) от количества легирующего цинка обнаружили [8], что они не монотонны: ход зависимостей резко меняется в районах ~1.5 ат.% Zn и ~6.0 ат.% Zn.
Структурная обусловленность такого поведения оптических свойств ниобата лития была установлена также сотрудниками института [9]. Причина оказалась в том, что при увеличении количества цинка дважды (в районах его концентраций 1.5 ат.% и 6.0 ат.%) меняется способ вхождения цинка в кристалл. Сначала при концентрациях до 1.5 ат.% цинк изоморфно замещает избыточный ниобий. Так как валентность цинка два (Zn+2), а ниобия пять (Nb+5), при каждом акте замещения для компенсации разности в валентностях три вакансии заселяются литием (исчезают). При получении кристалла состава (Li0.970Zn0.015}0.015)NbO3 весь избыточный ниобий оказывается исчерпанным.
Дальнейшее увеличение количества цинка требует иного механизма реализации. Цинк Zn+2 начинает замещать литий Li+1 в его позициях. При этом параллельно в кристалле увеличивается число вакансий в пропорции: одна новая вакансия на каждое замещение лития цинком. Этот процесс продолжается до концентрации цинка в твердом растворе 6.0 ат.% и образования кристаллов состава (Li0.88Zn0.06}0.06)NbO3. Продолжить наращивание количества цинка позволяет то, что он вновь вытесняет ниобий, но уже из основных позиций. Здесь, как и на первом этапе, со скоростью 3:1 вакансии заселяются литием и образуются кристаллы типа (Li0.91Zn0.06}0.03)(Nb0.99Zn0.01)O3. Данный механизм естественным образом заканчивается при количестве цинка в кристалле 8 ат.% и образовании соединения состава (Li0.94Zn0.06)(Nb0.98Zn0.02). В этих кристаллах больше нет вакансий, заселение которых литием могло бы компенсировать дальнейшее гетеровалентное замещение ниобия цинком.
Существование кристаллов с самокомпенсацией было предсказано на основании модельных расчетов. Вырастить кристаллы с несколько бOльшим содержанием цинка, чем 8 ат.%, удается, но их однородность и оптические свойства существенно ухудшаются. Указанные выше границы концентраций в зависимости от условий выращивания монокристаллов и наличия микропримесей могут несколько смещаться, но способы вхождения цинка в ниобат лития сменяют друг друга в той же последовательности, как было показано прецизионными структурными исследованиями.
Ультразвук в парателлурите
Кристаллы парателлурита a-TeO2 широко применяются в акустооптике. Созданные на их основе линии задержки используют тот факт, что поперечная плоскополяризованная ультразвуковая волна, распространяющаяся в монокристалле по направлениям [110] или [11Д0], оказывается достаточно медленной. Эти направления отвечают диагоналям основания тетрагональной элементарной ячейки кристалла. Парателлурит кристаллизуется в рамках ацентричной тетрагональной пространственной группы симметрии P43212 c параметрами элементарной ячейки а=4.810 Е, с=7.613 A (рис.5,а). Внимание специалистов-структурщиков привлекла в этих кристаллах весьма существенна анизотропия поглощения ультразвука [10]. Например, при распространении плоскополяризованной волны частотой в 1 Ггц вдоль направления [110] с колебаниями в волне по направлению [11Д0] поглощение достигает 290 дБ/см. Стоит кристалл повернуть на 45° вокруг оси симметрии четвертого порядка так, чтобы волна ультразвука пошла вдоль направления [100] с колебаниями по [010], как поглощение падает до 19 дБ/см. Если же монокристалл опрокинуть и колебания в волне совпадут по направлению с четверной осью симметрии кристалла, то при любом направлении распространения волны в перпендикулярной этому направлению плоскости (001) поглощение составит всего 9 дБ/см.
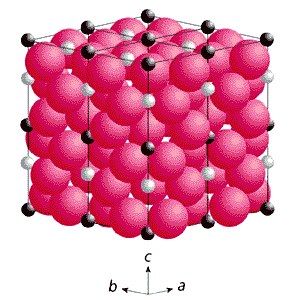
Рис. 4. Идеальная структура ниобата лития LiNbO3.
Цветные атомы кислорода образуют плотнейшую гексагональную упаковку.
Катионы ниобия (темные) и лития (светлые) упорядоченно заселяют октаэдрические полости кислородной упаковки.Для установления структурной причины такой резкой зависимости поглощения акустической волны от направления ее распространения были выполнены прецизионные рентгеноструктурные исследования монокристаллов a-TeO2. Окружение атома Те кислородами имеет тип 2+2+2, что означает (рис.5,б): два ближайших атома О отстоят от теллура на расстояниях 1.880 A (правые), два следующих кислорода удалены на 2.121 A (средние) и еще два атома О находятся на расстояниях 2.867 A.
Через общие атомы кислорода все группы [TeO6] объединены в трехмерный каркас. При этом каждый атом О связан с тремя атомами Те: от одного теллура кислород находится на близком расстоянии, от второго на среднем и от третьего - на увеличенном расстоянии. Такое распределение химических связей в кристалле обусловлено электронной структурой атомов Те. Потенциалы атом-атомного взаимодействия в кристаллах существенно несимметричны. Для сближения атомов по сравнению с равновесным расстоянием требуется больше усилий, чем для растяжения соответствующей химической связи. В пределе это означает, что нельзя вдавить атом в атом, но вполне реально разорвать химическую связь, скажем, нагреванием до температуры плавления кристаллического образца.
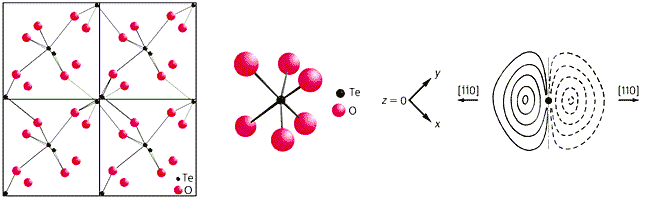
Рис. 5. Cтруктура парателлурита a-TeO2.
а - Проекция структуры вдоль оси c.
б - Ближайшее окружение атома Te атомами O.
в - Распределение ангармонической составляющей тепловых колебаний атома Te в плоскости (001) кристалла.
Представлена ангармоническая составляющая плотности вероятности нахождения атома Те в данной точке пространства.Окружение теллура кислородом, показанное на рис.5,б, существенно влияет на тепловые колебания атомов Те. Короткие (сильные) связи Те–О сжать значительно труднее, чем удлиненные (слабые) связи. В этом причина существенного ангармонизма тепловых колебаний теллура. По сравнению с гармоническими колебаниями атом Те в процессе теплового движения проводит относительно меньше времени, сближаясь с теми атомами О, которые имеют сильные связи с ним. Самое слабое сопротивление атом Те испытывает при сближении с наиболее удаленными кислородными соседями.
Уточнение атомной структуры a-TeO2 по рентгеновским дифракционным данным с учетом анизотропии и ангармонизма тепловых колебаний атомов позволило построить для атомов Те ангармоническую составляющую плотности вероятности нахождения в данной точке пространства в процессе теплового движения (рис.5,в). Максимум распределения смещен от равновесного положения атома Те по направлению [1Д1Д0]. В обратном направлении фиксируется минимум такого распределения. Разумеется, с учетом гармонической составляющей тепловых колебаний вероятность во всех точках оказывается положительной. Ангармоническая и гармоническая составляющие в направлении [110] соотносятся как 1:7, в направлении [100] это отношение становится 1:12, а в направлении [001] с точностью наших определений тепловые колебания теллура на 100% гармонические.
Таким образом, анизотропия поглощения гармонической ультразвуковой волны коррелирует с распределением в пространстве ангармонической составляющей тепловых колебаний атомов Те. Поглощение акустических волн оказывается минимальным, когда колебания в волне совпадают с направлением [001], в котором отсутствует заметный ангармонизм в тепловых колебаниях теллура.
Несколько заключительных слов
Современные дифракционные методы исследования атомной структуры кристаллических материалов позволяют с высокой точностью фиксировать тонкие детали их строения. Примененные к рядам изоструктурных соединений с изоморфными замещениями, эти методы дают надежную информацию о структурной обусловленности физических свойств кристаллов. Как показано выше на примерах суперионных кристаллов и кристаллических материалов с нелинейными оптическими характеристиками, такие знания открывают пути целенаправленного регулирования этих свойств методом изоморфных замещений. Понимание связей структура-свойства ведет к принципиально новому эффективному использованию данных, накопленных в постоянно пополняемых банках кристаллографической информации. Если вы знаете структурную обусловленность интересующего вас физического свойства, то банк кристаллографических данных выдаст вам списки кристаллов, обладающих необходимыми структурными характеристиками. Естественно, что именно эти кристаллы будут наиболее перспективными при поиске материалов с заданными свойствами.
Прецизионные структурные исследования важны не только для материаловедения. Физика твердого тела нуждается в такой информации при переходе от феноменологического описания свойств кристаллов и явлений, происходящих в них при внешних воздействиях, к их микроскопической теории.
Литература
1. Иванов-Шиц А.К., Мурин И.В. Ионика твердого тела. СПб., 2000.
2. Демьянец Л.Н., Доронин С.Н., Иванов-Шиц А.К. и др. Твердый электролит: Авторское свидетельство №1190885 на изобретение. 1985 г., 8 июля.
3. Максимов Б.А., Мурадян Л.А., Баданов Н.Н. и др. // Кристаллография. 1991. Т.36. №6. С.1431-1440.
4. Лосевская Т.Ю., Харитонова Е.П., Воронкова В.И. и др. // Кристаллография. 1999. Т.44. №1. С.95-97.
5. Yanovskii V.K., Voronkova V.I., Losevskaya T.Yu. et al. // Crystallography Reports. 2002. V.47, Suppl.1. P.S99-S104.
6. Черная Т.С., Волк Т.Р., Верин И.А. и др. // Кристаллография. 2002. Т.47. №2. С.249-252.
7. Abrahams S.C., Marsh P. // Acta Cryst. 1986. V.B42. P.61-68.
8. Volk T., Maximov B., Chernaya T. et al. // Appl. Phys. 2001. V.B72. P.647-652.
9. Черная Т.С., Максимов Б.А., Волк Т.Р. и др. // Письма в ЖЭТФ. 2001. Т.73. Вып.2. С.110-113.
10. Кондратюк И.П., Мурадян Л.А., Писаревский Ю.В. и др. // Кристаллография. 1987. Т.32. Вып.3. С.609-617.